05/02/2022
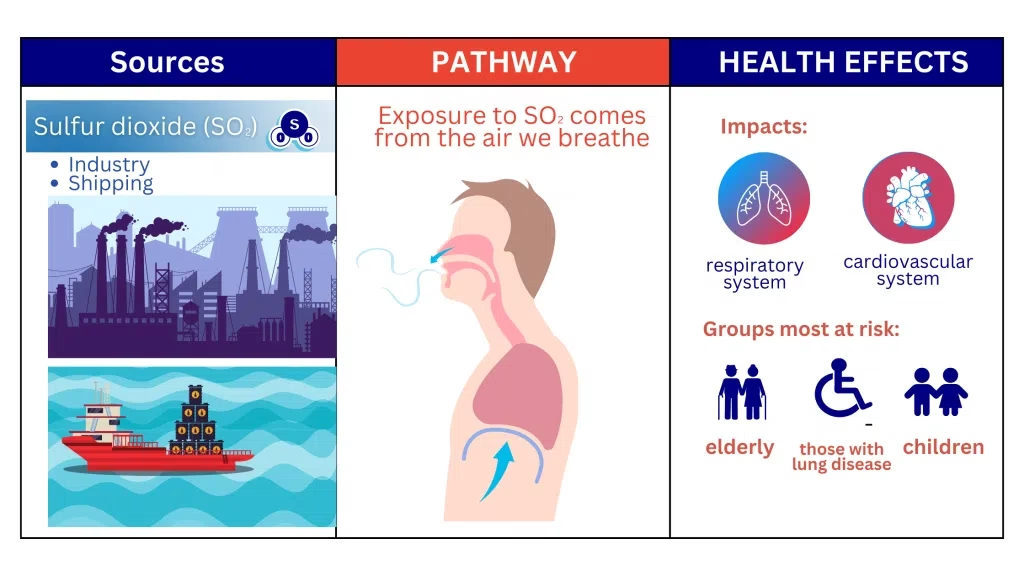
O dióxido de enxofre, mais conhecido pela sua fórmula química SO2 ou anidrido sulfuroso, é um gás de presença notável tanto na natureza quanto nas atividades humanas. Sua origem remonta a eventos vulcânicos e, de forma mais predominante, à queima de combustíveis fósseis e a processos industriais diversos. Este composto inorgânico, embora invisível e de odor forte, possui uma relevância imensa, sendo um pilar em certas aplicações industriais, como a produção de ácido sulfúrico, mas também um agente de preocupação significativa devido aos seus impactos adversos na qualidade do ar e na saúde humana.
Compreender as características e o comportamento do dióxido de enxofre é fundamental para avaliar seu papel no ecossistema e na segurança ocupacional. Estamos falando de um poluente atmosférico que, em concentrações elevadas, pode transformar-se em uma ameaça silenciosa, afetando desde a vegetação e a vida aquática até monumentos históricos e, crucialmente, a saúde respiratória de milhões de pessoas. Mergulhe conosco nesta análise detalhada para desvendar as propriedades, os perigos e os usos desse gás complexo e multifacetado.
- Propriedades Físicas e Químicas do Dióxido de Enxofre (SO2)
- A Estrutura Molecular do SO2: Por Que é Tão Solúvel?
- Fontes de Emissão e Ocorrência do Dióxido de Enxofre
- Dióxido de Enxofre e a Qualidade do Ar: O Desafio da Poluição
- O Impacto do SO2 na Saúde Humana: Doenças Respiratórias e Mais
- Aplicações Industriais do Dióxido de Enxofre: Usos e Cuidados
- Medidas de Segurança e Monitoramento em Ambientes Industriais
Propriedades Físicas e Químicas do Dióxido de Enxofre (SO2)
O dióxido de enxofre é um gás que, à temperatura ambiente, se manifesta em estado gasoso. Suas propriedades físicas são bastante distintivas: possui uma temperatura de fusão em torno de -72°C e uma temperatura de ebulição de aproximadamente -10°C, o que o torna um gás volátil mesmo em climas temperados. É incolor, o que dificulta sua detecção visual, mas seu odor forte e pungente é um alerta de sua presença em concentrações mais elevadas. Além disso, é um gás denso, o que significa que tende a se acumular em áreas mais baixas em ambientes confinados, e não é inflamável, o que é uma característica importante para sua manipulação industrial.
Uma das propriedades mais notáveis do SO2 é sua alta solubilidade em água. Essa característica é crucial para entender tanto suas aplicações quanto seus impactos ambientais e na saúde. Quando em contato com a água, o dióxido de enxofre reage para formar ácido sulfuroso, que, por sua vez, pode oxidar-se a ácido sulfúrico, um dos principais componentes da chuva ácida. Essa reatividade com a água é a base para muitos de seus efeitos tóxicos no corpo humano, especialmente nas mucosas úmidas do sistema respiratório e dos olhos. É, portanto, um gás polar, uma característica intrínseca à sua estrutura molecular.
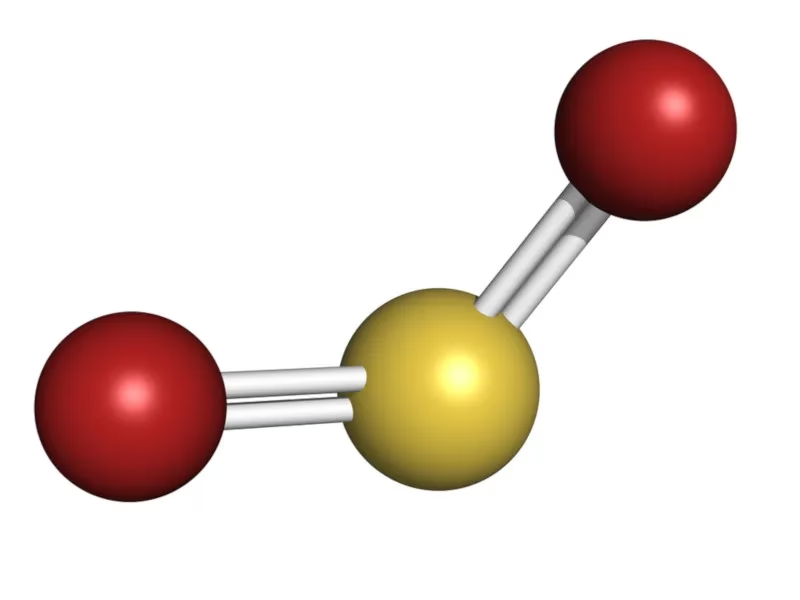
A Estrutura Molecular do SO2: Por Que é Tão Solúvel?
Para entender a alta solubilidade do dióxido de enxofre em água e sua reatividade, é essencial examinar sua estrutura molecular. O SO2 é um composto covalente, ou seja, é formado pela ligação entre dois ametais: um átomo de enxofre e dois átomos de oxigênio. Sua fórmula estrutural revela que o átomo de enxofre está ligado a ambos os átomos de oxigênio, formando uma geometria molecular angular. Essa configuração angular, em vez de linear, é o que confere ao dióxido de enxofre sua característica polar.
A polaridade de uma molécula é determinada pela distribuição desigual de cargas elétricas em sua estrutura. No caso do SO2, a diferença de eletronegatividade entre o enxofre e o oxigênio, combinada com a geometria angular (que não permite que os momentos de dipolo se anulem), resulta em uma molécula com uma extremidade ligeiramente positiva e outra ligeiramente negativa. Essa polaridade é o que permite que o dióxido de enxofre interaja fortemente com moléculas de água, que também são polares (a famosa regra "semelhante dissolve semelhante"). É essa afinidade com a água que facilita sua absorção e dissolução em tecidos biológicos úmidos e na atmosfera, desencadeando as reações que levam aos seus efeitos tóxicos e ambientais.
Fontes de Emissão e Ocorrência do Dióxido de Enxofre
As fontes de emissão de dióxido de enxofre na atmosfera são diversas e podem ser categorizadas em naturais e antropogênicas (resultantes da atividade humana). Entre as fontes naturais, as erupções vulcânicas são as mais significativas, liberando grandes quantidades de SO2 na atmosfera. No entanto, são as atividades humanas que contribuem com a maior parte das emissões globais.
A principal fonte antropogênica é a queima de combustíveis fósseis, como carvão mineral e óleo diesel, em usinas termelétricas, veículos e processos industriais. Esses combustíveis contêm enxofre como impureza, que, ao ser queimado, reage com o oxigênio do ar para formar dióxido de enxofre. Outras atividades industriais que liberam SO2 incluem a fabricação de fertilizantes, a produção de papel, a fundição de metais e refinarias de petróleo. Em muitos desses processos, o enxofre é utilizado ou é um subproduto inevitável. O transporte e manuseio do dióxido de enxofre, quando usado industrialmente, é tipicamente feito na forma de gás liquefeito, exigindo precauções rigorosas devido à sua toxicidade e volatilidade.
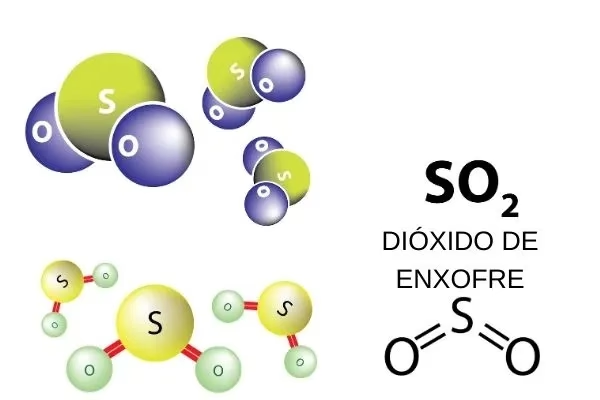
Dióxido de Enxofre e a Qualidade do Ar: O Desafio da Poluição
A emissão de dióxido de enxofre na atmosfera é um dos principais fatores que contribuem para a deterioração da qualidade do ar, com consequências abrangentes para o meio ambiente e a saúde pública. A ligação mais direta e devastadora do SO2 com a qualidade do ar é a formação da chuva ácida. Quando o dióxido de enxofre é liberado na atmosfera, ele reage com a água, oxigênio e outras substâncias químicas para formar ácido sulfúrico e ácido nítrico. Essas substâncias caem na Terra na forma de chuva, neve, neblina ou mesmo poeira seca, resultando na chuva ácida.
Os impactos da chuva ácida são múltiplos e severos:
- Ecossistemas aquáticos: A acidificação de rios e lagos altera o pH da água, tornando-a inóspita para muitas espécies de peixes e outros organismos aquáticos, prejudicando o crescimento populacional e a biodiversidade.
- Vegetação: Plantas e florestas são diretamente afetadas. A chuva ácida danifica as folhas, retarda o crescimento, torna as árvores mais suscetíveis a doenças e pragas, e pode até mesmo levar à morte de grandes áreas florestais.
- Solos: Aumenta a acidez do solo, o que pode lixiviar nutrientes essenciais e liberar metais tóxicos, que são então absorvidos pelas plantas.
- Estruturas e monumentos: Em centros urbanos e locais históricos, a acidez corrói materiais de construção, como mármore, calcário e metais, causando danos irreparáveis a edifícios, estátuas e infraestruturas.
Devido a esses perigos, o dióxido de enxofre foi incorporado aos parâmetros de qualidade do ar por órgãos reguladores em todo o mundo, como o Conselho Nacional do Meio Ambiente (CONAMA) no Brasil. Esses parâmetros estabelecem valores de concentrações máximas permitidas para diversos poluentes, incluindo o SO2, com o objetivo de preservar o meio ambiente e a saúde dos indivíduos. Por exemplo, em algumas regiões, como Goiás, limites específicos são definidos, como uma concentração média anual de 60 μg/m3 e uma concentração máxima diária de 200 μg/m3 para óxidos de enxofre em geral. O monitoramento contínuo é essencial para garantir que esses limites sejam respeitados e para implementar medidas de controle de emissões.
O Impacto do SO2 na Saúde Humana: Doenças Respiratórias e Mais
O dióxido de enxofre é um gás tóxico com efeitos significativos e prejudiciais à saúde humana, agindo principalmente nas mucosas úmidas do corpo. A exposição ao SO2 ocorre predominantemente por via inalatória, e seus efeitos podem variar de irritações leves a condições médicas graves, dependendo da concentração e do tempo de exposição. Ao entrar em contato com as superfícies úmidas do trato respiratório (nariz, garganta, pulmões) e dos olhos, o SO2 reage com a água para formar ácido sulfuroso e, subsequentemente, ácido sulfúrico. Essa reação ácida é a responsável pela maior parte dos danos observados.
Os sintomas iniciais e mais comuns da exposição ao SO2 incluem:
- Irritação no nariz, garganta e olhos.
- Tosse persistente.
- Náuseas.
- Falta de ar ou dificuldade respiratória.
- Produção excessiva de secreção.
- Crises de asma, especialmente em indivíduos asmáticos.
Em concentrações mais elevadas ou em exposições prolongadas, os efeitos podem ser muito mais severos. O gás pode causar inflamação aguda no sistema respiratório, levando a problemas cardíacos e dificuldades severas na respiração. Casos extremos podem resultar em queimaduras nas mucosas, edema de glote (inchaço na garganta que pode bloquear as vias aéreas), confusão mental, ansiedade e vômitos. A inibição do transporte mucociliar, um mecanismo natural de defesa dos pulmões, torna o sistema respiratório mais vulnerável a infecções e outras substâncias nocivas.
Indivíduos com doenças crônicas pulmonares, como asma, bronquite ou enfisema, e aqueles com problemas cardíacos são particularmente suscetíveis aos efeitos do dióxido de enxofre, podendo ter suas condições agravadas. Embora o dióxido de enxofre não seja classificado como cancerígeno, a exposição crônica pode levar a sequelas graves e permanentes, como bronquite crônica, broncopneumonia química, alterações permanentes do olfato e um declínio significativo das funções pulmonares. O contato direto do SO2 com os olhos pode causar conjuntivite química e lesões na córnea, enquanto a ingestão (raro, mas possível em ambientes industriais contaminados) pode resultar em dor abdominal, ulcerações na gengiva e erosões dentárias. A maior parte do SO2 inalado é metabolizada pelo fígado em sulfatos, que são excretados na urina, mas a exposição constante pode levar à sensibilização ao produto.
Aplicações Industriais do Dióxido de Enxofre: Usos e Cuidados
Apesar de seus riscos ambientais e de saúde, o dióxido de enxofre desempenha um papel crucial em diversas indústrias devido às suas propriedades químicas. Sua aplicação mais proeminente é no processo de produção de ácido sulfúrico (H2SO4), um dos produtos químicos industriais mais importantes e amplamente utilizados no mundo. O SO2 serve como um intermediário essencial nesse processo, sendo oxidado a trióxido de enxofre (SO3) e, em seguida, reagindo com água para formar o ácido.
Além da fabricação de ácido sulfúrico, o dióxido de enxofre é empregado em outras aplicações industriais significativas:
- Metalurgia: É utilizado como agente redutor, especialmente na extração de metais como o cobre e o níquel, onde ajuda a remover impurezas de óxidos metálicos.
- Branqueamento: Devido às suas propriedades redutoras, o SO2 é um agente branqueador eficaz para materiais como papel, tecidos e lã, embora seu uso tenha diminuído em algumas aplicações devido a preocupações ambientais.
- Conservante de alimentos e vinhos: O dióxido de enxofre é empregado como conservante e antioxidante na indústria alimentícia, especialmente na produção de vinhos (onde é conhecido como sulfitos), frutas secas e vegetais, para prevenir a oxidação e o crescimento microbiano. No entanto, seu uso é regulamentado devido à sensibilidade de algumas pessoas a sulfitos.
- Desinfetante e fumigante: Suas propriedades antimicrobianas o tornam útil como desinfetante e para fumigação em armazéns e instalações agrícolas, ajudando a controlar pragas e microrganismos.
- Purificação de derivados de petróleo: Na indústria de refino de petróleo, o SO2 pode ser usado para purificar certos derivados, removendo impurezas.
O transporte e manuseio do dióxido de enxofre para essas aplicações exigem protocolos de segurança rigorosos, pois é um gás tóxico e corrosivo quando em contato com a umidade. É crucial que as indústrias que o utilizam ou o produzem como subproduto implementem sistemas de controle de emissões e monitoramento rigoroso para proteger trabalhadores e o meio ambiente.

Medidas de Segurança e Monitoramento em Ambientes Industriais
Dada a toxicidade e os riscos associados ao dióxido de enxofre, a segurança no trabalho e o monitoramento ambiental são de suma importância em qualquer indústria que lide com esse gás. A exposição inalatória é a principal via de contato, o que torna a qualidade do ar em ambientes de trabalho uma prioridade absoluta. Para garantir a segurança dos trabalhadores e a conformidade com as regulamentações, são estabelecidos limites de exposição ocupacional.
Exemplos de limites de exposição incluem:
- Limite de Exposição Permitido (TWA - Time-Weighted Average): Geralmente, em um período de 8 horas, o limite é de 0,5 partes por milhão (ppm).
- Limite de Exposição de Curto Prazo (STEL - Short-Term Exposure Limit): Para uma exposição máxima de 15 minutos, o limite é de 1 ppm.
- Imediatamente Perigoso à Vida e Saúde (IDLH - Immediately Dangerous to Life or Health): Concentrações de 100 ppm são consideradas imediatamente perigosas à vida e saúde, exigindo evacuação imediata ou uso de equipamentos de proteção respiratória autônomos.
Para manter a exposição a níveis seguros, diversas medidas de controle são implementadas:
- Sistemas de Ventilação: Adequados sistemas de ventilação local e geral são essenciais para diluir e remover o SO2 do ambiente de trabalho.
- Detecção de Gás: A instalação de detectores de gás fixos em pontos estratégicos do ambiente de risco é fundamental. Esses detectores devem ser posicionados considerando a densidade do SO2 (que é mais denso que o ar e tende a se acumular em áreas baixas), o potencial de difusão e os padrões de ventilação. Alarmes devem ser configurados para alertar os trabalhadores sobre concentrações elevadas.
- Detectores Portáteis: Além dos sistemas fixos, detectores portáteis de SO2 são excelentes ferramentas de segurança. Eles podem ser usados por trabalhadores em áreas de risco para monitoramento pessoal contínuo e como backup em caso de suspeita de falha dos detectores fixos ou em locais onde a fixação não é viável.
- Equipamento de Proteção Individual (EPI): Em situações onde a exposição não pode ser totalmente controlada por engenharia, o uso de EPI adequado, como respiradores com filtros específicos para gases ácidos ou máscaras autônomas, é mandatório. Óculos de segurança e luvas também são importantes para evitar o contato com a pele e os olhos.
- Treinamento e Procedimentos de Emergência: Os trabalhadores devem ser treinados sobre os riscos do SO2, os sintomas de exposição, os procedimentos de emergência, o uso correto do EPI e as ações a serem tomadas em caso de vazamento ou exposição acidental. Planos de resposta a emergências devem estar em vigor.
- Manutenção Preventiva: Inspeções e manutenções regulares dos equipamentos que manuseiam SO2, bem como dos sistemas de ventilação e detecção, são cruciais para prevenir vazamentos e garantir a funcionalidade dos controles.
A implementação dessas medidas é vital para proteger a saúde dos trabalhadores e garantir um ambiente de trabalho seguro e produtivo. A atenção constante aos níveis de SO2 e a prontidão para agir em caso de emergência são pilares da gestão de riscos químicos.
Perguntas Frequentes sobre o Dióxido de Enxofre
Para consolidar o conhecimento sobre o dióxido de enxofre, compilamos algumas das perguntas mais frequentes:
O que é dióxido de enxofre (SO2)?
O dióxido de enxofre, ou anidrido sulfuroso, é um gás incolor com odor forte, denso e não inflamável, cuja fórmula química é SO2. É um óxido inorgânico que se forma principalmente pela queima de combustíveis fósseis e atividades industriais, além de ocorrências naturais como erupções vulcânicas. É altamente solúvel em água e considerado um poluente atmosférico tóxico.
Como o dióxido de enxofre afeta a saúde humana?
O SO2 é um gás tóxico que afeta principalmente o sistema respiratório e os olhos. Ao entrar em contato com as mucosas úmidas, forma ácidos que causam irritação, tosse, náuseas, dificuldade respiratória e irritação ocular. Em altas concentrações, pode provocar inflamação aguda, problemas cardíacos, queimaduras e, a longo prazo, bronquite crônica e declínio da função pulmonar. Pessoas com doenças respiratórias ou cardíacas pré-existentes são mais vulneráveis.
Onde o dióxido de enxofre é utilizado industrialmente?
O dióxido de enxofre tem várias aplicações industriais importantes. Sua principal utilização é na produção de ácido sulfúrico. Além disso, é empregado como agente redutor na metalurgia, branqueador para papel e tecidos, conservante em alimentos e vinhos (sulfitos), desinfetante e fumigante, e na purificação de derivados de petróleo.
Qual a relação entre o SO2 e a chuva ácida?
O dióxido de enxofre é um dos principais precursores da chuva ácida. Uma vez liberado na atmosfera, ele reage com a água e outras substâncias para formar ácido sulfúrico. Este ácido, juntamente com o ácido nítrico (formado a partir de óxidos de nitrogênio), cai na Terra como precipitação ácida, causando danos significativos a ecossistemas aquáticos, florestas, solos e estruturas construídas pelo homem.
Como a concentração de dióxido de enxofre no ar é monitorada?
A concentração de SO2 é monitorada por órgãos ambientais por meio de redes de estações de qualidade do ar que utilizam analisadores instrumentais. Em ambientes industriais, são utilizados detectores de gás fixos e portáteis para garantir que os níveis de exposição ocupacional permaneçam dentro dos limites de segurança estabelecidos por regulamentações como as do CONAMA e agências de saúde ocupacional. O monitoramento contínuo é essencial para proteger a saúde pública e o meio ambiente.
Se você quiser conhecer outros artigos parecidos com Dióxido de Enxofre: Propriedades, Perigos e Usos, pode visitar a categoria Saúde.