21/08/2025
No vasto e complexo cenário da biologia humana, a comunicação celular é um pilar fundamental para a manutenção da vida. Cada célula do nosso corpo, de alguma forma, precisa interagir e responder a sinais químicos para coordenar funções vitais. É nesse contexto que surgem os receptores farmacológicos, proteínas extraordinárias que atuam como os principais elementos de percepção desse intrincado sistema de comunicação química. A compreensão desses receptores não é apenas uma curiosidade científica, mas a pedra angular sobre a qual a farmacologia moderna foi construída, permitindo-nos desvendar os mecanismos pelos quais os medicamentos exercem seus efeitos biológicos e, consequentemente, desenvolver terapias cada vez mais eficazes e seguras.
A ideia da existência de receptores, inicialmente uma hipótese audaciosa, ganhou força a partir de observações cruciais sobre a ação dos fármacos. Três características notáveis foram particularmente determinantes: a alta potência, ou seja, a capacidade de pequenas quantidades de uma substância produzirem grandes efeitos; a especificidade química, onde apenas certas moléculas se ligam a determinados alvos; e a especificidade biológica, que se manifesta na capacidade de um fármaco produzir efeitos distintos em diferentes tecidos ou tipos celulares. Essas evidências apontavam para a existência de componentes celulares específicos com os quais os fármacos interagiam, como chaves que se encaixam em fechaduras moleculares. A partir dessa premissa, os farmacologistas passaram a explorar a natureza dessa interação, culminando em descobertas que revolucionaram a medicina e o desenvolvimento de novos tratamentos.
Para que um fármaco exerça sua ação, é indispensável que ocorra uma interação entre ele e o receptor, formando o que se denomina complexo fármaco-receptor. Essa ligação pode variar em sua natureza e duração, sendo classificada principalmente em reversível ou irreversível. A ligação reversível, caracterizada por forças intermoleculares mais fracas (como ligações iônicas, pontes de hidrogênio e forças de Van der Waals), é a mais comum. Ela permite que o fármaco se ligue ao receptor, exerça seu efeito e, posteriormente, se dissocie, liberando o receptor para novas interações. Essa dinâmica é crucial para a regulação dos efeitos dos medicamentos no corpo, permitindo que a intensidade da resposta seja modulada pela concentração do fármaco.
Por outro lado, a ligação irreversível envolve a formação de ligações covalentes fortes e duradouras entre o fármaco e o receptor. Uma vez formada, essa ligação é extremamente estável e a dissociação do fármaco do receptor é mínima ou inexistente. Nesses casos, a recuperação da função do receptor geralmente depende da síntese de novas proteínas receptoras pela célula, um processo que pode levar horas ou até dias. Embora menos comum, a ligação irreversível é empregada em certos tratamentos, como no caso de alguns inibidores de enzimas que atuam de forma "suicida", bloqueando permanentemente a atividade da proteína alvo. A natureza da ligação fármaco-receptor é um fator determinante na duração e na intensidade da resposta farmacológica, influenciando diretamente a posologia e a segurança dos medicamentos.
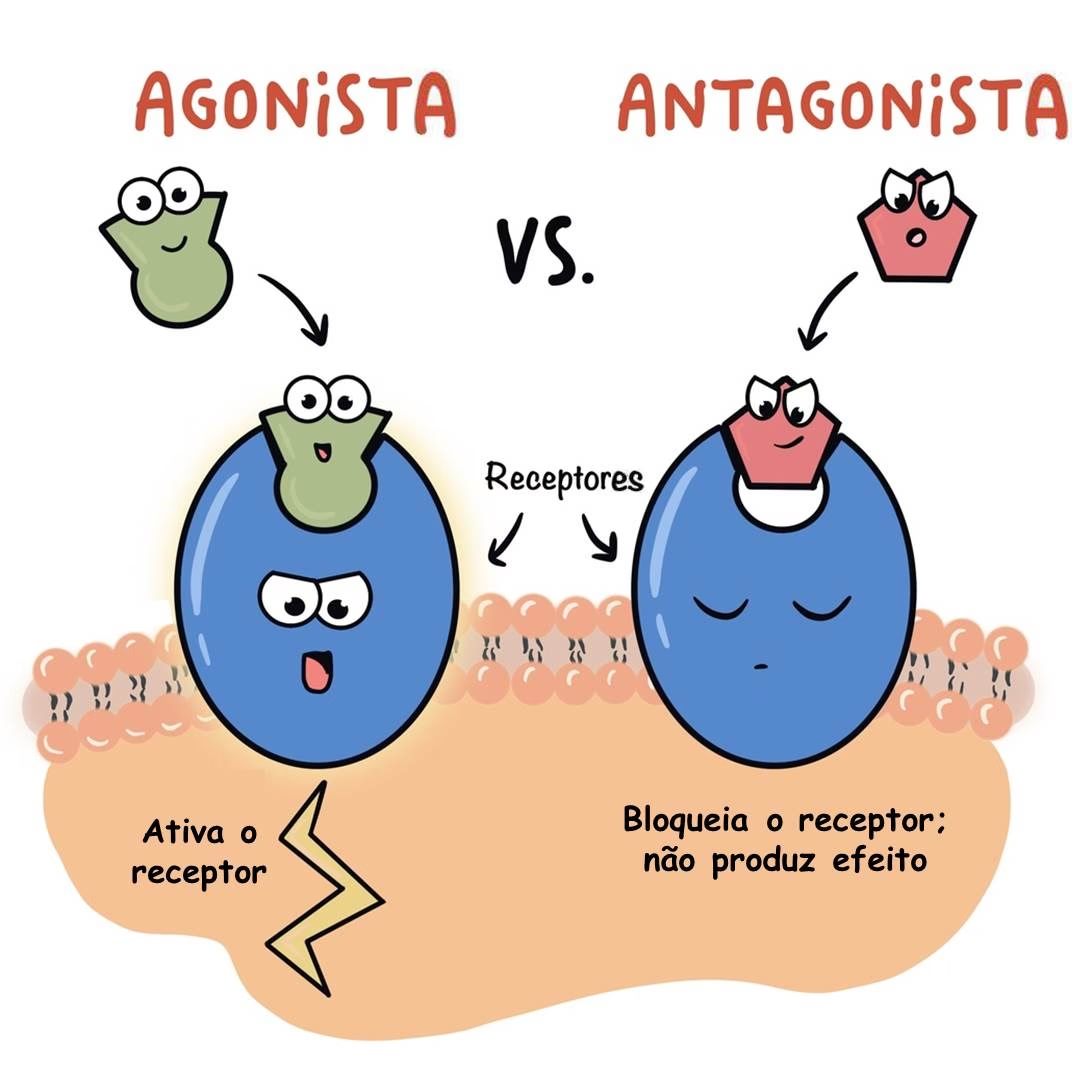
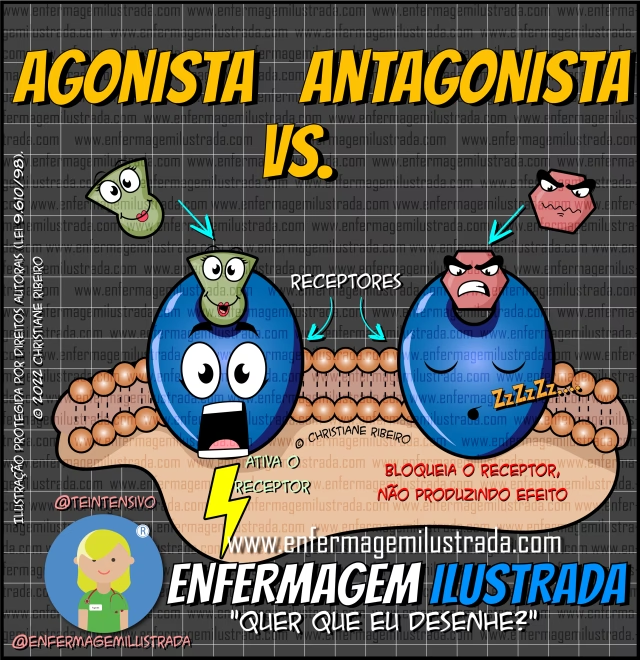
A interação entre um fármaco e seu receptor não é apenas uma questão de ligação, mas também de como essa ligação influencia a função do receptor. Diversos modelos conceituais, incluindo o modelo de dois estados, propõem que os receptores podem existir em diferentes estados conformacionais de equilíbrio, sendo os principais o estado ativo e o inativo. A capacidade de um fármaco de estabilizar ou alterar esse equilíbrio é o que define seu papel como agonista ou antagonista.
Um agonista é um fármaco que, ao se ligar ao receptor, favorece a conformação ativa, mimetizando ou potencializando a ação de uma substância endógena (produzida pelo próprio corpo). Os agonistas possuem afinidade pelo receptor (capacidade de se ligar) e eficácia intrínseca (capacidade de produzir uma resposta biológica). Eles podem ser classificados em:
- Agonistas totais: Produzem a resposta máxima possível quando ocupam todos os receptores.
- Agonistas parciais: Mesmo ocupando todos os receptores, produzem uma resposta submáxima em comparação com um agonista total. Podem atuar como antagonistas em presença de um agonista total.
- Agonistas inversos: Estabilizam a conformação inativa de receptores que apresentam atividade constitutiva (alguma atividade mesmo na ausência de ligantes).
Em contraste, um antagonista é um fármaco que se liga ao receptor, mas não o ativa. Sua principal função é impedir a ativação do receptor por um agonista (seja ele endógeno ou exógeno). Os antagonistas possuem afinidade pelo receptor, mas não possuem eficácia intrínseca. Eles podem ser:
- Antagonistas competitivos: Ligam-se ao mesmo sítio de ligação do agonista de forma reversível. Podem ser superados pelo aumento da concentração do agonista.
- Antagonistas não competitivos: Ligam-se a um sítio diferente do receptor, alterando sua conformação e impedindo a ligação ou a ativação do agonista, ou ligam-se irreversivelmente ao mesmo sítio. Não podem ser superados pelo aumento da concentração do agonista.
- Antagonistas químicos: Inativam o agonista diretamente, sem envolver um receptor.
- Antagonistas fisiológicos: Produzem um efeito oposto ao do agonista através de um mecanismo ou receptor diferente.
A distinção entre agonistas e antagonistas é crucial na terapêutica, pois determina se um medicamento irá ativar uma via de sinalização (como a adrenalina em receptores beta-adrenérgicos para tratar choque) ou bloqueá-la (como os beta-bloqueadores em receptores beta-adrenérgicos para tratar hipertensão).
Com base em sua estrutura molecular, mecanismos de transdução de sinal e tempo de ação, os receptores farmacológicos podem ser categorizados em quatro principais superfamílias. Essa classificação é fundamental para entender a diversidade de respostas celulares e o desenvolvimento de fármacos direcionados.
1. Receptores Canais Iônicos (Ligand-Gated Ion Channels)
Estes receptores são proteínas transmembrana que formam um poro através da membrana celular. Sua ativação, geralmente pela ligação de um neurotransmissor, resulta na abertura ou fechamento do canal iônico, permitindo o fluxo rápido de íons (como Na+, K+, Ca2+, Cl-) através da membrana. Isso leva a uma alteração no potencial de membrana da célula, resultando em respostas celulares muito rápidas, na ordem de milissegundos. São cruciais na transmissão sináptica no sistema nervoso.
- Exemplos: Receptor nicotínico de acetilcolina (nAChR), receptor GABA-A, receptor NMDA.
- Fármacos alvos: Benzodiazepínicos (potencializam GABA-A), anestésicos locais (bloqueiam canais de sódio), relaxantes musculares (bloqueiam nAChR).
2. Receptores Acoplados à Proteína G (GPCRs)
Constituem a maior e mais diversa superfamília de receptores, com mais de 800 membros conhecidos no genoma humano. São proteínas transmembrana que atravessam a membrana celular sete vezes (daí o nome "receptores serpentina"). Sua ativação pela ligação de um ligante extracelular desencadeia uma série de eventos intracelulares complexos. O receptor ativado interage com uma proteína G heterotrimérica (composta por subunidades alfa, beta e gama), que por sua vez ativa ou inibe enzimas efetoras (como adenilato ciclase, fosfolipase C) ou canais iônicos. Isso leva à produção de segundos mensageiros (como AMP cíclico, diacilglicerol, IP3, íons cálcio), que modulam a atividade de proteínas intracelulares e, finalmente, a resposta celular. As respostas mediadas por GPCRs são mais lentas que as dos canais iônicos, na ordem de segundos a minutos, mas são amplificadas e diversificadas.
- Exemplos: Receptores adrenérgicos (alfa e beta), receptores muscarínicos de acetilcolina, receptores de dopamina, serotonina, histamina.
- Fármacos alvos: Beta-bloqueadores (propranolol), agonistas beta-2 (salbutamol), anti-histamínicos, opioides.
3. Receptores Ligados a Enzimas (Enzyme-Linked Receptors)
Também conhecidos como receptores tirosina quinase (RTKs) ou receptores ligados à quinase, são proteínas transmembrana que possuem um domínio extracelular de ligação ao ligante e um domínio intracelular com atividade enzimática intrínseca, ou que se associa a enzimas. Geralmente, a ligação do ligante (frequentemente fatores de crescimento, hormônios como a insulina ou citocinas) causa a dimerização do receptor e a ativação da atividade tirosina quinase, que fosforila resíduos de tirosina em proteínas intracelulares. Essa fosforilação serve como um sinal para uma cascata de eventos de sinalização, incluindo vias como MAPK/ERK, PI3K/Akt e JAK/STAT, que regulam processos celulares como crescimento, proliferação, diferenciação e metabolismo. As respostas são mais lentas que as dos GPCRs, na ordem de minutos a horas.
- Exemplos: Receptor de insulina, receptores de fatores de crescimento (EGF, PDGF, VEGF), receptores de citocinas.
- Fármacos alvos: Inibidores de tirosina quinase (imatinib para câncer), anticorpos monoclonais que bloqueiam a ligação de ligantes (trastuzumabe para câncer de mama).
4. Receptores Nucleares (Intracellular Receptors)
Diferentemente das outras superfamílias, os receptores nucleares são proteínas solúveis localizadas no citoplasma ou no núcleo da célula, e não na membrana celular. Seus ligantes são tipicamente moléculas lipofílicas que podem atravessar a membrana plasmática, como hormônios esteroides (estrogênio, testosterona, cortisol), hormônios tireoidianos, vitamina D e retinoides. Uma vez que o ligante se liga ao receptor, o complexo ligante-receptor se transloca para o núcleo (se já não estiver lá) e se liga a sequências específicas de DNA (elementos de resposta hormonal) em regiões promotoras de genes. Isso modula a transcrição gênica, aumentando ou diminuindo a síntese de proteínas específicas. As respostas mediadas por receptores nucleares são as mais lentas, levando horas ou até dias para se manifestar, mas são de longa duração, pois envolvem alterações na expressão gênica.
- Exemplos: Receptor de estrogênio, receptor de androgênio, receptor de glicocorticoide, receptor de hormônio tireoidiano.
- Fármacos alvos: Tamoxifeno (antiestrogênio para câncer de mama), prednisona (glicocorticoide para inflamação), contraceptivos orais.
Essa diversidade de receptores permite que o corpo responda a uma vasta gama de sinais químicos com diferentes velocidades e magnitudes, garantindo a homeostase e a adaptação a estímulos externos.
Tabela Comparativa das Superfamílias de Receptores Farmacológicos
| Característica | Canais Iônicos | GPCRs | Receptores Ligados a Enzimas | Receptores Nucleares |
|---|---|---|---|---|
| Localização | Membrana Plasmática | Membrana Plasmática | Membrana Plasmática | Citoplasma/Núcleo |
| Estrutura | Poro transmembrana | Sete domínios transmembrana | Um domínio transmembrana, domínio enzimático intracelular | Proteína solúvel |
| Ligantes Típicos | Neurotransmissores (ACh, GABA) | Hormônios, Neurotransmissores, Peptídeos | Fatores de Crescimento, Insulina, Citocinas | Hormônios Esteroides/Tireoidianos, Vitaminas Lipossolúveis |
| Mecanismo de Ação | Fluxo direto de íons | Ativação de Proteína G, segundos mensageiros | Atividade enzimática (quinase) intrínseca ou associada | Modulação da Transcrição Gênica |
| Tempo de Resposta | Milissegundos | Segundos a Minutos | Minutos a Horas | Horas a Dias |
| Exemplos de Efeitos | Potenciais de ação, contração muscular rápida | Contração muscular lenta, secreção glandular, modulação cardíaca | Crescimento celular, proliferação, metabolismo | Diferenciação celular, desenvolvimento, metabolismo de longo prazo |
A importância dos receptores farmacológicos transcende sua função como alvos de medicamentos; eles são componentes vitais para a homeostase do organismo. Consequentemente, distúrbios em sua função ou estrutura podem levar ao desenvolvimento de diversas patologias. A disfunção receptora pode ocorrer por mutações genéticas que alteram a proteína, por doenças autoimunes que produzem anticorpos contra os receptores, ou por regulação inadequada (down-regulation ou up-regulation) em resposta a estímulos crônicos.
Um exemplo clássico de doença autoimune envolvendo receptores é a miastenia gravis. Nesta condição, o sistema imunológico produz anticorpos que atacam e destroem os receptores nicotínicos de acetilcolina na junção neuromuscular. A redução no número de receptores funcionais impede a transmissão eficaz dos sinais nervosos para os músculos, resultando em fraqueza muscular progressiva e fadiga.
Outro exemplo proeminente é o diabetes mellitus insulino-dependente (Tipo 1), embora seja principalmente uma doença autoimune que destrói as células beta do pâncreas produtoras de insulina, existem também casos de resistência à insulina (Tipo 2) onde os receptores de insulina nas células-alvo se tornam menos sensíveis ou em menor número. Embora o diabetes Tipo 2 seja multifatorial, a disfunção do receptor de insulina desempenha um papel crucial na patogênese da doença, levando à incapacidade das células de captar glicose do sangue, resultando em hiperglicemia crônica.
Esses exemplos sublinham a intrínseca ligação entre a saúde dos receptores e a saúde geral do indivíduo, destacando a relevância de se entender a fundo a biologia desses alvos terapêuticos.
Perguntas Frequentes sobre Receptores Farmacológicos
Para aprofundar seu conhecimento sobre o tema, respondemos algumas das perguntas mais comuns:
O que é afinidade e eficácia intrínseca?
Afinidade refere-se à capacidade de um fármaco se ligar ao seu receptor. Quanto maior a afinidade, menor a concentração do fármaco necessária para ocupar os receptores. A eficácia intrínseca, por outro lado, é a capacidade do complexo fármaco-receptor de produzir uma resposta biológica. Um agonista tem alta afinidade e alta eficácia intrínseca, enquanto um antagonista tem afinidade, mas eficácia intrínseca nula.
Todos os fármacos atuam em receptores?
Não, embora a maioria o faça. Alguns fármacos atuam por mecanismos não receptores, como antiácidos que neutralizam o ácido estomacal, diuréticos osmóticos que alteram a osmolaridade, ou agentes quelantes que se ligam a íons metálicos tóxicos. No entanto, a grande maioria dos medicamentos com ação específica age através da interação com receptores.
O que significa "regulação" de receptores (up-regulation e down-regulation)?
As células podem alterar o número ou a sensibilidade de seus receptores em resposta a estímulos prolongados. "Up-regulation" é o aumento do número ou da sensibilidade dos receptores, geralmente em resposta a uma exposição crônica a um antagonista ou à privação de um ligante endógeno. "Down-regulation" é a diminuição do número ou da sensibilidade dos receptores, tipicamente em resposta à exposição crônica a um agonista, para evitar uma superestimulação constante e proteger a célula de danos.
Como a pesquisa em receptores está evoluindo?
A pesquisa em receptores farmacológicos está em constante evolução. Avanços em biologia molecular, genômica e proteômica permitem a identificação de novos receptores, a caracterização de suas estruturas tridimensionais com alta precisão e a compreensão de suas interações em nível atômico. Isso possibilita o design racional de fármacos, onde moléculas são projetadas especificamente para se encaixar em sítios de ligação de receptores, maximizando a seletividade e minimizando efeitos colaterais. A farmacogenômica, por exemplo, estuda como as variações genéticas nos receptores de um indivíduo podem influenciar a resposta aos medicamentos, abrindo caminho para a medicina personalizada.
É possível um fármaco se ligar a mais de um tipo de receptor?
Sim, muitos fármacos exibem um certo grau de "promiscuidade" na ligação, interagindo com múltiplos tipos de receptores, especialmente se forem estruturalmente semelhantes. Essa falta de seletividade completa é frequentemente a causa de efeitos colaterais indesejados. O objetivo no desenvolvimento de novos fármacos é maximizar a seletividade para o receptor alvo, a fim de obter o efeito terapêutico desejado com o mínimo de reações adversas.
Em síntese, os receptores farmacológicos representam o elo crucial entre as moléculas de fármacos e as respostas biológicas que observamos. Desde as primeiras hipóteses sobre sua existência até a detalhada classificação em superfamílias com mecanismos de ação distintos, o entendimento desses componentes celulares tem sido uma jornada de descobertas contínuas. A interação droga-receptor, seja ela reversível ou irreversível, agonista ou antagonista, é o cerne da farmacodinâmica, determinando a potência, a especificidade e a duração da ação de um medicamento.
A capacidade de modular a função desses receptores é o que nos permite tratar uma vasta gama de doenças, desde infecções até condições crônicas como hipertensão e diabetes. No entanto, a própria disfunção dos receptores pode ser a causa de patologias, como visto na miastenia gravis. A pesquisa incessante nesse campo, impulsionada por novas tecnologias e abordagens multidisciplinares, continua a aprofundar nosso conhecimento e a expandir as possibilidades terapêuticas. Podemos considerar, com base no vasto levantamento de obras e autores que permeiam este campo, que os conceitos e as aplicações dos receptores farmacológicos estão em constante evolução. Essa dinâmica nos permite crer que, num futuro não muito distante, será possível não apenas refinar a dosagem de componentes químicos das drogas de maneira cada vez mais subjetiva e precisa, mas também desenvolver terapias altamente personalizadas, otimizando a eficácia e minimizando os riscos para cada indivíduo. A farmacologia está, de fato, caminhando para um cenário de avanços cada vez mais notáveis, com os receptores no centro dessa revolução.
Se você quiser conhecer outros artigos parecidos com Receptores Farmacológicos: Chaves da Ação Medicamentosa, pode visitar a categoria Farmacologia.