12/08/2025
O Trióxido de Enxofre (SO₃), frequentemente referido como anidrido sulfúrico ou óxido sulfúrico, é uma das moléculas mais intrigantes e impactantes no estudo da química e do meio ambiente. Sua presença, quer seja como um subproduto industrial ou como um componente reativo na atmosfera, desencadeia uma série de efeitos que merecem nossa atenção. Este composto singular, formado por ligações duplas covalentes entre átomos de enxofre (S) e oxigênio (O), possui uma fórmula molecular simples, SO₃, mas suas propriedades físicas e químicas são complexas e de grande relevância, especialmente quando consideramos sua interação com a saúde humana e os ecossistemas naturais.
Compreender o SO₃ é mergulhar em um universo onde a estrutura molecular dita o comportamento macroscópico, influenciando desde sua forma física em diferentes temperaturas até sua capacidade de transformar o clima e a qualidade do ar que respiramos. É um ácido de Lewis potente, um poluente atmosférico notório e um reagente essencial em diversos processos industriais. Suas características, como a geometria trigonal plana e a polaridade nula, são fundamentais para desvendar por que ele se comporta da maneira que se comporta, e por que sua regulação é tão crucial para a proteção ambiental e a saúde pública.
Propriedades Físicas Detalhadas do Trióxido de Enxofre
As propriedades físicas do trióxido de enxofre são a chave para entender seu comportamento e os desafios que ele representa. A começar por sua estrutura, o SO₃ adota uma geometria trigonal plana, com ângulos de 120º entre as ligações S=O. Essa simetria perfeita é a razão pela qual o momento dipolo da molécula é nulo, conferindo a ela um caráter intrinsecamente apolar. Essa apolaridade, embora possa parecer um detalhe técnico, influencia diretamente sua solubilidade em diferentes solventes e sua interação com outras moléculas, desempenhando um papel crucial em sua reatividade e transporte atmosférico.
Com uma massa molecular de 80,06 g/mol, o SO₃ é um composto relativamente leve, mas suas características físicas à temperatura ambiente são bastante distintas. O trióxido de enxofre possui pontos de fusão e ebulição notavelmente baixos: 16,9 ºC e 45 ºC, respectivamente. Isso significa que, em um dia quente de verão, ele pode facilmente passar do estado sólido para o líquido e, com um pouco mais de aquecimento, para o estado gasoso. À temperatura ambiente comum, ele é encontrado na forma de um líquido incolor e fumegante, com uma densidade de 1,92 kg/m³. O termo 'fumegante' não é uma mera descrição estética; ele denota a alta higroscopicidade do SO₃, que ao entrar em contato com a umidade do ar, reage vigorosamente para formar minúsculas gotículas de ácido sulfúrico, criando uma névoa visível. Essa densidade, consideravelmente maior que a da água, também tem implicações para seu manuseio e armazenamento seguros.
Uma das propriedades mais notáveis do SO₃ é sua higroscopicidade extrema. Ele tem uma afinidade tão forte pela água que seu calor de hidratação é capaz de provocar a ignição de materiais combustíveis como madeira ou algodão. Isso ocorre porque o SO₃ desidrata rapidamente os carboidratos presentes nas estruturas desses materiais, liberando calor suficiente para iniciar a combustão. Essa característica o torna um reagente perigoso e exige precauções rigorosas em qualquer ambiente onde seja manipulado.
| Propriedade | Valor/Característica |
|---|---|
| Fórmula Molecular | SO₃ |
| Massa Molecular | 80,06 g/mol |
| Geometria Molecular | Trigonal Plana |
| Polaridade | Apolar |
| Ponto de Fusão | 16,9 ºC |
| Ponto de Ebulição | 45 ºC |
| Densidade (líquido) | 1,92 kg/m³ |
| Estado à Temperatura Ambiente | Líquido incolor fumegante |
| Caráter | Ácido de Lewis forte |
| Higroscopicidade | Muito alta |
Reatividade e Incompatibilidade
A estabilidade do SO₃, embora aparente em sua forma pura, é rapidamente comprometida na presença de certas substâncias. Ele é um composto estável termodinamicamente, mas sua reatividade química é notável. O SO₃ é incompatível com uma vasta gama de materiais, incluindo matéria orgânica, metais, bases e cianetos, com os quais reage de forma forte e muitas vezes perigosa. Sua interação com a água e o oxigênio atmosférico é particularmente significativa, pois essas reações estão na raiz de seus impactos ambientais.
Como um ácido de Lewis, o SO₃ é um ávido receptor de elétrons, sendo um ácido mais forte que o dióxido de enxofre (SO₂). Essa característica é fundamental para sua principal reação de interesse ambiental e industrial: a formação de ácido sulfúrico (H₂SO₄) em contato com a água, conforme a equação: SO₃(g) + H₂O(l) → H₂SO₄(l). Essa reação exotérmica é a base para a produção industrial de ácido sulfúrico, uma das commodities químicas mais importantes do mundo, mas também explica seu papel central na formação da chuva ácida.
Métodos de Obtenção do Trióxido de Enxofre
A produção de trióxido de enxofre é um processo de grande importância industrial, principalmente devido à sua utilização na síntese de ácido sulfúrico. O método mais comum e economicamente viável é o chamado Processo de Contato, que envolve a oxidação do dióxido de enxofre (SO₂) purificado com oxigênio atmosférico. Essa reação ocorre em temperaturas elevadas, geralmente entre 400 e 600 ºC, e exige a presença de um catalisador para acelerar o processo sem ser consumido na reação. O pentóxido de vanádio (V₂O₅) é o catalisador mais empregado, frequentemente ativado com óxido de potássio e suportado em terra diatomácea ou sílica para maximizar a área de superfície e a eficiência.
A reação do Processo de Contato, 2SO₂(g) + O₂(g) ⇌ 2SO₃(g), é reversível e exotérmica, o que significa que um aumento na temperatura pode deslocar o equilíbrio no sentido da formação dos reagentes (SO₂ e O₂), diminuindo o rendimento de SO₃. Para otimizar a produção, é crucial operar em temperaturas controladas e, por vezes, utilizar catalisadores adicionais. Por exemplo, a adição de catalisadores à base de nitrato de potássio pode tornar a reação mais rápida, minimizando a perda de SO₃ e garantindo uma conversão eficiente do SO₂. Um exemplo de reação alternativa com catalisador é: SO₂ + NO₂ → SO₃ + NO.
Além do Processo de Contato, o SO₃ pode ser gerado por outros meios, alguns dos quais são menos controláveis e contribuem para a poluição ambiental. A combustão de compostos sulfetados, que ocorre nas chaminés de fábricas e usinas termelétricas, é uma fonte significativa de SO₃ liberado na atmosfera. Em escala de laboratório, o trióxido de enxofre pode ser produzido pela reação de pirólise do bissulfato de sódio (NaHSO₄). Este processo em duas etapas envolve a desidratação do bissulfato de sódio a 315 ºC para formar pirossulfato de sódio (Na₂S₂O₇) e água (2 NaHSO₄ → Na₂S₂O₇ + H₂O), seguido pelo craqueamento do pirossulfato de sódio a 460 ºC para liberar SO₃ e sulfato de sódio (Na₂SO₄): Na₂S₂O₇ → Na₂SO₄ + SO₃.
Impactos do Trióxido de Enxofre na Saúde Humana
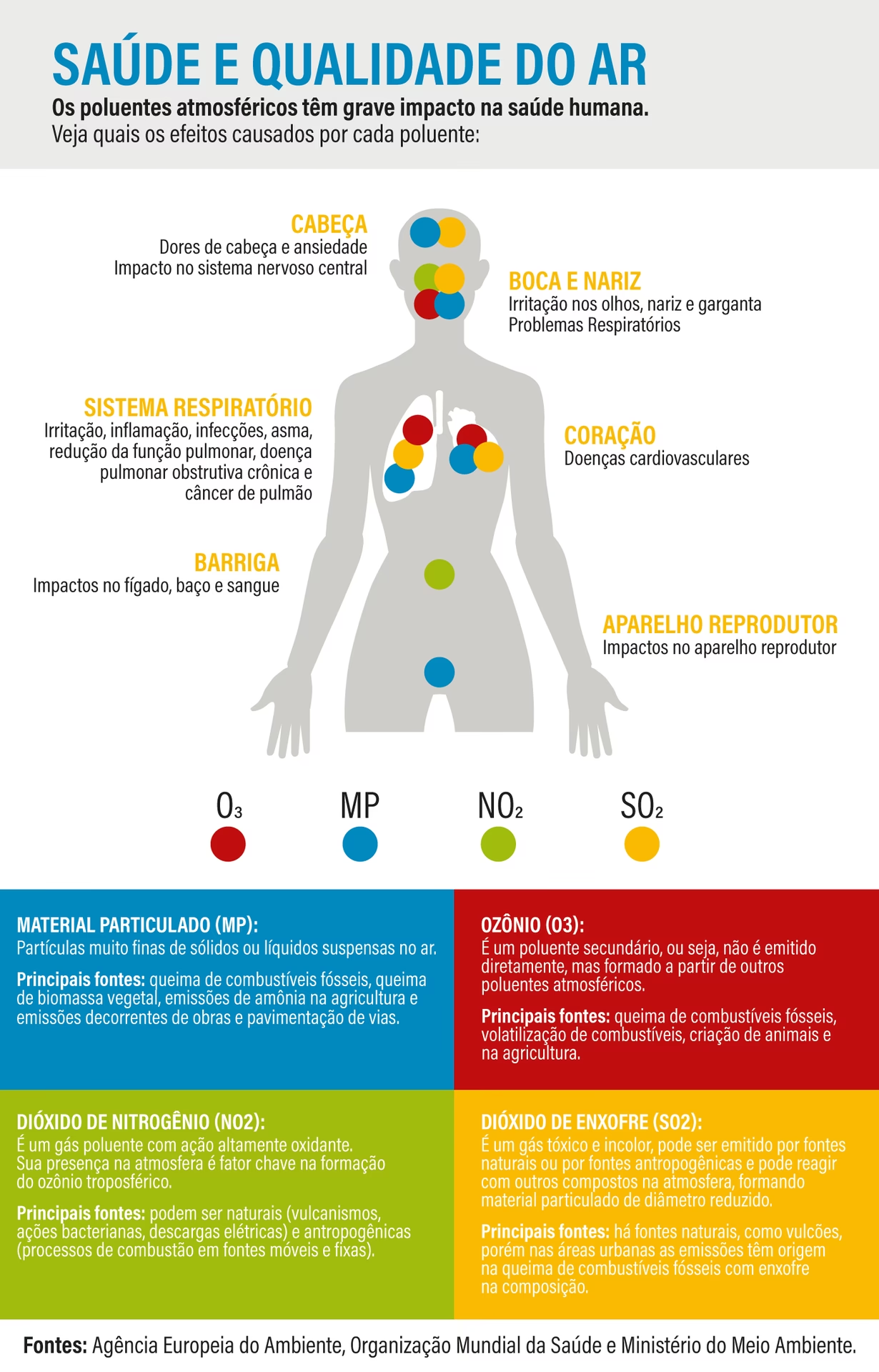
Apesar de sua utilidade industrial, a presença do SO₃ na atmosfera, mesmo em baixas concentrações, representa uma séria ameaça à saúde humana. Sendo um composto gasoso irritante e corrosivo, o SO₃ é facilmente inalado e, devido à sua alta reatividade com a umidade, transforma-se rapidamente em ácido sulfúrico nas vias respiratórias. Este ácido forte ataca as membranas mucosas, causando inflamação e danos aos tecidos.
Os problemas de saúde mais comuns associados à exposição ao SO₃ são as doenças respiratórias. Desde irritações leves na garganta e nos olhos até condições mais graves, como bronquites agudas e crônicas, o SO₃ compromete a função pulmonar. A exposição prolongada ou a concentrações elevadas pode levar a danos pulmonares irreversíveis, incluindo o enfisema pulmonar, uma condição debilitante que reduz drasticamente a capacidade respiratória. Além dos efeitos diretos no sistema respiratório, estudos indicam que a exposição ao SO₃ e aos aerossóis de sulfato formados a partir dele também pode agravar ou causar problemas cardiovasculares, aumentando o risco de ataques cardíacos e derrames, especialmente em indivíduos já vulneráveis.
A gravidade desses impactos na saúde é tal que o trióxido de enxofre, juntamente com outros óxidos de enxofre (SOx), está incluído na lista de indicadores da qualidade do ar monitorados por órgãos reguladores como o Conselho Nacional de Meio Ambiente (CONAMA) no Brasil. A vigilância e o controle das emissões de SO₃ são, portanto, medidas essenciais para a proteção da saúde pública e a promoção de um ambiente saudável.
O Trióxido de Enxofre e a Chuva Ácida: Um Desafio Ambiental
Um dos impactos ambientais mais conhecidos e devastadores do trióxido de enxofre é sua contribuição para a formação da chuva ácida. Como mencionado, o SO₃ reage prontamente com a água presente na atmosfera (nuvens, neblina, vapor d'água) para formar ácido sulfúrico (H₂SO₄), um ácido forte e altamente corrosivo. Este ácido, uma vez formado, dissolve-se nas gotículas de água atmosféricas e precipita na forma de chuva, neve, neblina ou mesmo poeira ácida, diminuindo significativamente o pH da água da chuva.
A precipitação ácida causa uma série de problemas ambientais e materiais. Nos ecossistemas aquáticos, a diminuição do pH da água afeta a vida aquática, tornando-a tóxica para peixes, anfíbios e invertebrados, e alterando o equilíbrio biológico. Nos solos, a chuva ácida lixivia nutrientes essenciais, como cálcio e magnésio, e libera metais tóxicos, como o alumínio, que podem ser prejudiciais para as plantas e a vida microbiana do solo, comprometendo a fertilidade e a biodiversidade. Florestas inteiras podem ser danificadas e até destruídas pela exposição prolongada à chuva ácida, que enfraquece as árvores, tornando-as mais suscetíveis a doenças e pragas.
Além dos impactos biológicos, a chuva ácida causa danos significativos em ambientes urbanos e infraestruturas. Monumentos históricos, edificações, pontes e veículos são corroídos e desfigurados pelo ácido sulfúrico. A beleza de estátuas de mármore e a integridade de estruturas metálicas são comprometidas, resultando em perdas culturais e econômicas substanciais. Tintas e revestimentos também são degradados, acelerando a deterioração de bens e exigindo manutenção constante. A presença do SO₃ na atmosfera é, portanto, um grave problema de higião ambiental que exige ações contínuas de controle e mitigação.
Medidas de Controle e Prevenção das Emissões de SO₃
Dada a natureza poluente e corrosiva do trióxido de enxofre e seus derivados, o controle de suas emissões é uma prioridade global para a proteção da saúde humana e do meio ambiente. As estratégias de controle focam principalmente nas fontes industriais, que são os maiores emissores de SO₂ e, consequentemente, de SO₃.
Uma das principais abordagens é a dessulfurização dos gases de exaustão, que envolve a remoção do dióxido de enxofre antes que ele seja liberado na atmosfera. Isso é frequentemente feito por meio de lavadores de gases (scrubbers) que utilizam soluções alcalinas, como calcário (carbonato de cálcio) ou hidróxido de cálcio, para reagir com o SO₂ e formar sulfato de cálcio (gesso), um subproduto que pode ter usos industriais. Outras tecnologias incluem a adsorção de SO₂ em leitos sólidos e a conversão catalítica para produtos menos nocivos.
Além das tecnologias de pós-combustão, a prevenção na fonte é fundamental. Isso inclui o uso de combustíveis com baixo teor de enxofre em usinas termelétricas e indústrias, bem como a otimização de processos industriais para reduzir a formação de óxidos de enxofre. A implementação de padrões de emissão rigorosos e a fiscalização por parte de órgãos ambientais são cruciais para garantir que as indústrias adotem e mantenham essas tecnologias e práticas.
A conscientização pública sobre os perigos do SO₃ e da chuva ácida também desempenha um papel importante. Informar a população sobre as fontes de poluição, os impactos na saúde e no meio ambiente, e as medidas que podem ser tomadas para mitigar esses problemas, ajuda a construir um apoio para políticas ambientais mais eficazes e a promover um comportamento mais sustentável.
Perguntas Frequentes sobre o Trióxido de Enxofre (SO₃)
O que é Trióxido de Enxofre (SO₃)?
O Trióxido de Enxofre, ou SO₃, é um composto químico inorgânico formado por um átomo de enxofre e três átomos de oxigênio. É um gás incolor ou líquido fumegante à temperatura ambiente, conhecido por sua alta reatividade e por ser um precursor do ácido sulfúrico.
Quais são os principais riscos do SO₃ para a saúde humana?
A exposição ao SO₃ pode causar graves problemas respiratórios, como irritação das vias aéreas, bronquite e, em casos mais graves, enfisema pulmonar. Também pode estar associado a problemas cardiovasculares e irritação nos olhos e na pele devido à sua natureza ácida e corrosiva.
Como o SO₃ contribui para a chuva ácida?
O SO₃ reage com a água e o vapor d'água na atmosfera para formar ácido sulfúrico (H₂SO₄). Este ácido forte se mistura com a precipitação (chuva, neve) e cai na Terra como chuva ácida, que é prejudicial a ecossistemas, vegetação e estruturas.
Onde o SO₃ é encontrado ou produzido?
O SO₃ é produzido principalmente como um intermediário na fabricação de ácido sulfúrico (através do Processo de Contato). Também é formado como um poluente atmosférico a partir da queima de combustíveis fósseis que contêm enxofre, como carvão e petróleo, em indústrias e usinas de energia.
É possível controlar a emissão de SO₃?
Sim, o controle das emissões de SO₃ (e SO₂) é realizado por meio de tecnologias de dessulfurização de gases de exaustão, como lavadores de gases, que removem os óxidos de enxofre antes que sejam liberados na atmosfera. O uso de combustíveis com baixo teor de enxofre e a otimização de processos industriais também são medidas preventivas importantes.
Se você quiser conhecer outros artigos parecidos com O SO3: Propriedades e Impacto Vital, pode visitar a categoria Saúde.

