04/12/2025
A forma como nosso corpo processa e elimina medicamentos é um campo fascinante e de extrema importância para a eficácia e segurança de qualquer tratamento farmacológico. Este processo, conhecido como biotransformação, é uma série de reações bioquímicas que alteram a estrutura química dos fármacos, preparando-os para a excreção. Embora o fígado seja o principal centro dessa atividade, uma complexa interação de fatores genéticos, fisiológicos e externos determina a velocidade e a extensão com que cada indivíduo metaboliza uma substância. Compreender esses fatores é fundamental para otimizar a terapia medicamentosa e minimizar os riscos de efeitos adversos.
- O Que É Biotransformação e Por Que Ela É Crucial?
- As Duas Fases da Biotransformação: Uma Orquestra Bioquímica
- Fatores que Moldam a Biotransformação Individual
- O Papel Vital dos Transportadores Hepáticos de Fármacos
- Cinética da Biotransformação: Como o Corpo Processa os Fármacos
- Impacto da Idade na Biotransformação
- Perguntas Frequentes (FAQ) sobre Biotransformação de Fármacos
- 1. O que é um profármaco?
- 2. Por que o fígado é tão importante na biotransformação?
- 3. Qual a diferença principal entre as reações da Fase I e da Fase II da biotransformação?
- 4. Como as interações medicamentosas afetam a biotransformação?
- 5. Quais são os perigos de ter um metabolismo muito rápido ou muito lento para um fármaco?
O Que É Biotransformação e Por Que Ela É Crucial?
A biotransformação, também chamada de metabolismo de fármacos, é o conjunto de processos pelos quais o organismo modifica quimicamente as substâncias exógenas, incluindo os medicamentos. O objetivo primordial dessas transformações é tornar os compostos mais polares e hidrossolúveis, facilitando sua eliminação pelos rins (na urina) ou pelo fígado (na bile). Classicamente, a biotransformação leva à inativação do fármaco, reduzindo seu efeito farmacológico. No entanto, é importante ressaltar que nem sempre esse é o caso. Alguns metabólitos gerados podem ser farmacologicamente ativos, e em certas situações, até mais potentes que o composto original. Quando uma substância inativa ou com pouca atividade é projetada especificamente para ser ativada por meio do metabolismo no corpo, ela é denominada profármaco. Essa estratégia é frequentemente utilizada para melhorar a absorção, a distribuição ou a seletividade do medicamento.
Os fármacos podem ser biotransformados por uma variedade de reações químicas, incluindo oxidação, redução, hidrólise, hidratação, conjugação, condensação ou isomerização. Embora as enzimas responsáveis por esses processos estejam presentes em diversos tecidos do corpo, sua maior concentração e atividade ocorrem no fígado, que é, de fato, o principal órgão metabolizador de fármacos. No entanto, outros órgãos, como os rins, o intestino e os pulmões, também contribuem para a biotransformação.
As Duas Fases da Biotransformação: Uma Orquestra Bioquímica
Para a maioria dos fármacos, a biotransformação ocorre em duas etapas distintas, mas frequentemente sequenciais, conhecidas como Fase I e Fase II. Essas fases trabalham em conjunto para garantir a eficiente eliminação dos medicamentos do organismo.
Reações da Fase I: A Preparação
As reações da Fase I são processos não sintéticos que envolvem a introdução ou modificação de um grupo funcional na molécula do fármaco, ou a clivagem de ligações existentes. As principais reações dessa fase são a oxidação, a redução e a hidrólise. O objetivo é geralmente aumentar a polaridade do fármaco, tornando-o mais reativo para as reações da Fase II, ou, em alguns casos, diretamente para a excreção. O sistema enzimático mais importante e amplamente estudado da Fase I é o citocromo P-450 (CYP450). Esta é uma superfamília de isoenzimas microssomais que desempenham um papel central na oxidação de uma vasta gama de fármacos. Os elétrons necessários para essas reações de oxidação são fornecidos pela NADPH–CYP450 redutase, uma flavoproteína que transfere elétrons do NADPH (nicotinamida adenina dinucleotídeo fosfato reduzida) para o sistema CYP450.
Reações da Fase II: A Conjugação
As reações da Fase II são processos sintéticos que envolvem a conjugação (união) do fármaco original ou de seu metabólito da Fase I com uma substância endógena (produzida pelo próprio corpo). Essas substâncias conjugadas são geralmente grandes, polares e hidrossolúveis, o que as torna muito mais fáceis de serem excretadas pelos rins (na urina) e pelo fígado (na bile). A reação de conjugação mais comum é a glucuronidação, que ocorre no sistema enzimático microssomal hepático. Outras reações de conjugação importantes incluem a acetilação e a sulfoconjugação. A conjugação com aminoácidos, como glutamina ou glicina, também produz conjugados que são prontamente excretados na urina. É importante notar que alguns fármacos podem ser submetidos apenas às reações da Fase I ou da Fase II, ou passar diretamente para a Fase II sem uma Fase I prévia. Portanto, a numeração das fases reflete uma classificação funcional, e não necessariamente uma sequência obrigatória.
Para ilustrar a diferença entre as fases, podemos considerar a seguinte comparação:
| Característica | Fase I (Não Sintética) | Fase II (Sintética/Conjugação) |
|---|---|---|
| Tipo de Reação | Oxidação, Redução, Hidrólise | Conjugação com substâncias endógenas |
| Objetivo Principal | Introduzir/modificar grupos funcionais, aumentar reatividade | Aumentar polaridade para excreção |
| Principais Enzimas | Citocromo P-450 (CYP450) | Glucuroniltransferases, Sulfotransferases, N-acetiltransferases, etc. |
| Produto Final | Metabólitos mais polares ou reativos | Conjugados altamente polares e hidrossolúveis |
| Localização Comum | Microssomas hepáticos | Microssomas hepáticos, citosol |
Fatores que Moldam a Biotransformação Individual
A taxa de biotransformação de fármacos pode variar drasticamente entre os pacientes, resultando em respostas terapêuticas muito diferentes. Em alguns indivíduos, o metabolismo pode ser tão rápido que as concentrações plasmáticas e teciduais eficazes não são alcançadas, comprometendo o tratamento. Em outros, o metabolismo pode ser excessivamente lento, levando ao acúmulo do fármaco e ao surgimento de efeitos tóxicos com as doses habituais. Essa variabilidade é influenciada por uma série de fatores cruciais.
Genética: A Assinatura Única de Cada Paciente
Os fatores genéticos são talvez os mais significativos na determinação da variabilidade individual na biotransformação de fármacos. Polimorfismos genéticos, que são variações no DNA de uma população, podem afetar a expressão e a função das enzimas metabolizadoras de fármacos, especialmente as isoenzimas do citocromo P-450. Por exemplo, algumas pessoas podem ter versões de enzimas CYP450 que funcionam mais rapidamente (metabolizadores ultrarrápidos) ou mais lentamente (metabolizadores lentos) do que a média. Essas diferenças genéticas explicam por que um medicamento pode ser altamente eficaz e seguro para uma pessoa, mas ineficaz ou tóxico para outra, mesmo na mesma dose. A farmacogenômica, o estudo de como os genes afetam a resposta de uma pessoa aos medicamentos, está se tornando cada vez mais importante para a medicina personalizada.
Condições de Saúde Coexistentes
A presença de certas doenças pode comprometer a capacidade do corpo de metabolizar fármacos. Hepatopatias crônicas, como cirrose ou hepatite, são particularmente impactantes, pois o fígado é o principal local de biotransformação. A redução da função hepática pode levar a uma diminuição significativa na taxa de metabolismo, prolongando a meia-vida dos fármacos e aumentando o risco de toxicidade. Da mesma forma, a insuficiência cardíaca avançada pode reduzir o fluxo sanguíneo para o fígado, diminuindo a entrega de fármacos às enzimas metabolizadoras e, consequentemente, afetando sua biotransformação.
Interações Medicamentosas: O Efeito Dominó
As interações entre fármacos são uma causa comum de variabilidade na biotransformação. Um medicamento pode induzir (aumentar a atividade) ou inibir (diminuir a atividade) as enzimas metabolizadoras de outro fármaco. A indução enzimática, por exemplo, pode levar a uma biotransformação mais rápida do segundo fármaco, resultando em níveis plasmáticos subterapêuticos e perda de eficácia. Por outro lado, a inibição enzimática pode reduzir o metabolismo do segundo fármaco, levando ao acúmulo e ao aumento do risco de toxicidade. O sistema CYP450 é um alvo frequente para essas interações, e muitos medicamentos comuns são conhecidos por serem indutores ou inibidores de suas isoenzimas específicas. Pacientes que utilizam múltiplos medicamentos devem ter suas interações avaliadas cuidadosamente para evitar efeitos adversos.
O Papel Vital dos Transportadores Hepáticos de Fármacos
Além das enzimas metabolizadoras, os transportadores hepáticos de fármacos desempenham um papel crucial na disposição, metabolismo e eliminação de medicamentos pelo fígado. Essas proteínas, localizadas nas células parenquimatosas hepáticas, são responsáveis por mover as moléculas de fármacos para dentro (influxo) e para fora (efluxo) do fígado, bem como para a bile ou de volta para o sangue.
Existem dois tipos principais de transportadores:
- Transportadores de Influxo: Translocam moléculas do sangue para dentro das células hepáticas, permitindo que o fármaco acesse as enzimas metabolizadoras.
- Transportadores de Efluxo: Medeiam a excreção de fármacos e seus metabólitos para a bile (para eliminação fecal) ou de volta para o sangue (para eliminação renal).
Assim como as enzimas, os transportadores hepáticos de fármacos também podem ser afetados por polimorfismos genéticos. Variações genéticas podem alterar a expressão ou a função desses transportadores, influenciando a concentração de fármacos no fígado e no sangue. Por exemplo, portadores de certos genótipos de transportadores podem apresentar níveis séricos aumentados de estatinas (medicamentos para colesterol), tornando-os mais suscetíveis à miopatia induzida por estatina. A compreensão desses transportadores é vital para prever a resposta individual aos fármacos e evitar reações adversas.
Cinética da Biotransformação: Como o Corpo Processa os Fármacos
A forma como a taxa de biotransformação se relaciona com a concentração do fármaco no corpo é descrita pela cinética de eliminação, que pode ser de primeira ordem ou de ordem zero.
Cinética de Primeira Ordem
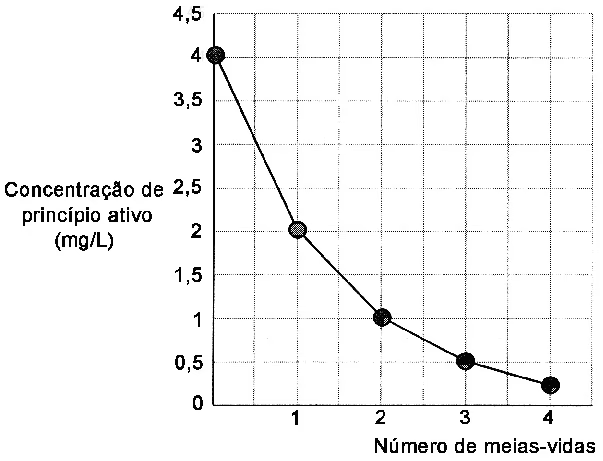
Para a maioria dos fármacos e em concentrações terapêuticas habituais, a biotransformação ocorre em uma taxa que é proporcional à concentração do fármaco presente no corpo. Isso significa que uma fração constante do fármaco é metabolizada por unidade de tempo. Este modelo é conhecido como eliminação de primeira ordem, ou cinética linear. Consequentemente, o fármaco possui uma meia-vida específica, que é o tempo necessário para que a concentração plasmática do fármaco seja reduzida pela metade. Por exemplo, se houverem 500 mg de um fármaco no corpo no tempo zero e sua meia-vida for de 1 hora, após 1 hora haverá 250 mg, e após 2 horas, 125 mg. A maioria dos fármacos segue essa cinética, o que permite prever com razoável precisão seus níveis no organismo ao longo do tempo.
Cinética de Ordem Zero
Em contraste, quando a concentração de um fármaco é muito alta, a maioria dos sítios das enzimas metabolizadoras pode ficar ocupada. Nesse ponto, a biotransformação ocorre na sua taxa máxima e não aumenta mais com o aumento da concentração do fármaco. Uma quantidade fixa de fármaco é biotransformada por unidade de tempo, independentemente de quão alta seja a concentração total. Este fenômeno é conhecido como cinética de ordem zero, ou eliminação de capacidade limitada. Nesses casos, o fármaco não possui uma meia-vida específica, pois a taxa de eliminação é constante. Por exemplo, se houverem 500 mg de um fármaco no corpo no tempo zero e a depuração máxima for de 50 mg/hora, após 1 hora haverá 450 mg, e após 2 horas, 400 mg. À medida que a concentração do fármaco aumenta, a biotransformação pode mudar de cinética de primeira ordem para ordem zero, o que pode levar a um rápido acúmulo do fármaco no corpo e a um aumento inesperado dos efeitos tóxicos.
Impacto da Idade na Biotransformação
A idade é um fator significativo que influencia a capacidade do organismo de biotransformar fármacos, com implicações importantes tanto para neonatos quanto para idosos.
- Em Idosos: Com o envelhecimento, a capacidade do fígado para a biotransformação, especialmente por meio do sistema enzimático do citocromo P-450, pode reduzir-se em 30% ou mais. Essa redução é atribuída, em parte, à diminuição do volume hepático e do fluxo sanguíneo para o fígado. Consequentemente, fármacos que são principalmente biotransformados por esse sistema tendem a atingir níveis plasmáticos mais elevados e a ter meias-vidas prolongadas em pacientes idosos. Isso significa que doses habituais para adultos jovens podem ser excessivas para idosos, aumentando o risco de toxicidade. É por isso que frequentemente são necessárias doses menores e/ou intervalos de dosagem maiores para essa população.
- Em Neonatos: Os recém-nascidos possuem sistemas enzimáticos microssomais hepáticos que ainda estão em desenvolvimento parcial. Isso os torna menos eficientes na biotransformação de muitos fármacos. Um exemplo clássico é a dificuldade na glucuronidação, uma reação crucial da Fase II. A incapacidade de conjugar adequadamente certos fármacos pode levar a efeitos graves, como observado com o cloranfenicol, que em neonatos pode causar a “síndrome do bebê cinzento” devido ao acúmulo da droga. A imaturidade dos processos de biotransformação nos neonatos exige extrema cautela e ajuste de doses para evitar toxicidade.
Curiosamente, a glucuronidação, ao contrário de outros processos de Fase II e do sistema CYP450, não parece ser significativamente afetada pelo envelhecimento em adultos. Da mesma forma, a acetilação e a sulfoconjugação também não são processos que sofrem impacto considerável com o avanço da idade.
Perguntas Frequentes (FAQ) sobre Biotransformação de Fármacos
1. O que é um profármaco?
Um profármaco é uma substância que, por si só, é inativa ou tem pouca atividade farmacológica. Ela é projetada para ser biotransformada no corpo em um metabólito ativo, que então exerce o efeito terapêutico desejado. Isso é feito para melhorar características como absorção, distribuição ou redução de efeitos colaterais.
2. Por que o fígado é tão importante na biotransformação?
O fígado é o principal local de biotransformação de fármacos porque contém uma alta concentração das enzimas metabolizadoras, como o sistema citocromo P-450 e as enzimas de conjugação. Além disso, o fígado recebe diretamente o sangue do trato gastrointestinal (via veia porta), o que significa que muitos fármacos absorvidos passam pelo fígado antes de serem distribuídos para o resto do corpo, um fenômeno conhecido como metabolismo de primeira passagem.
3. Qual a diferença principal entre as reações da Fase I e da Fase II da biotransformação?
As reações da Fase I (não sintéticas) introduzem ou modificam grupos funcionais no fármaco (ex: oxidação, redução, hidrólise), tornando-o mais polar ou reativo. Já as reações da Fase II (sintéticas) envolvem a conjugação do fármaco ou de seu metabólito da Fase I com uma substância endógena (ex: glucuronidação, acetilação), resultando em um composto altamente polar e hidrossolúvel, pronto para excreção. A Fase I prepara, a Fase II finaliza a solubilização para eliminação.
4. Como as interações medicamentosas afetam a biotransformação?
As interações medicamentosas podem afetar a biotransformação de duas maneiras principais: indução ou inibição enzimática. A indução significa que um fármaco aumenta a atividade das enzimas que metabolizam outro fármaco, acelerando sua eliminação e podendo reduzir sua eficácia. A inibição, por outro lado, significa que um fármaco diminui a atividade dessas enzimas, retardando a eliminação do outro fármaco e aumentando o risco de acúmulo e toxicidade.
5. Quais são os perigos de ter um metabolismo muito rápido ou muito lento para um fármaco?
Se o metabolismo for muito rápido, o fármaco pode ser eliminado do corpo antes de atingir as concentrações terapêuticas eficazes, resultando em falha do tratamento. Se o metabolismo for muito lento, o fármaco pode se acumular no corpo, atingindo concentrações tóxicas e causando efeitos adversos graves. Ambos os cenários ressaltam a importância da individualização da terapia medicamentosa.
Em suma, a biotransformação de fármacos é um processo dinâmico e complexo, influenciado por uma intrincada rede de fatores. Desde a nossa composição genética única até as condições de saúde que enfrentamos e os outros medicamentos que utilizamos, cada elemento desempenha um papel na forma como nosso corpo lida com as substâncias que ingerimos. A compreensão desses mecanismos não apenas aprimora a segurança e a eficácia dos tratamentos farmacológicos, mas também abre caminho para uma medicina cada vez mais personalizada e precisa, onde a dosagem e a escolha do fármaco podem ser adaptadas às necessidades metabólicas de cada paciente. Manter-se informado sobre esses processos é um passo importante para otimizar sua saúde e bem-estar.
Se você quiser conhecer outros artigos parecidos com Biotransformação de Fármacos: Fatores Chave, pode visitar a categoria Farmacologia.